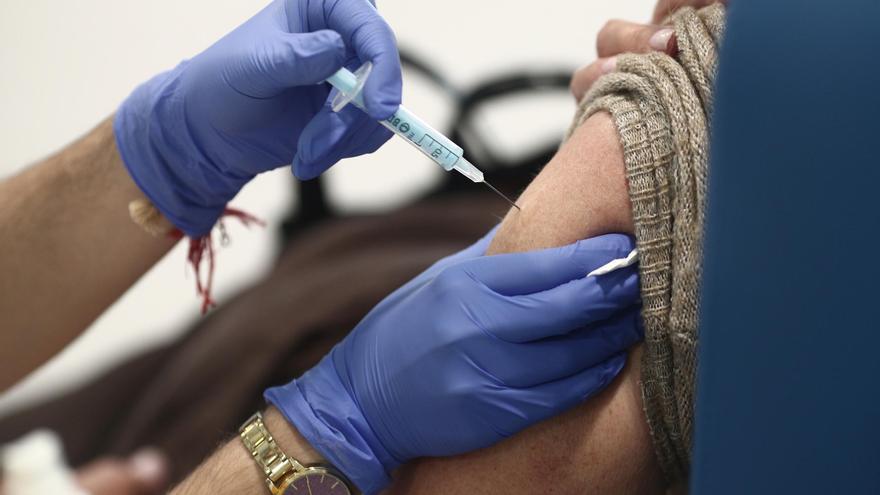
La vacuna española contra la covid, Bimervax, de la farmacéutica Hipra, se ha convertido en la primera de este tipo que recibe la precalificación de la Organización Mundial de la Salud (OMS), que es su sello de aprobación.
Según informa el laboratorio con sede en Amer (Girona), este certificado le permitirá llegar a países más allá de Europa, por lo que valoran positivamente el hito.
También aseguran que la precalificación encaja perfectamente con la vocación de servicio internacional con el que ha sido concebida Bimervax.
En este sentido, destacan que, “al ser una vacuna de proteína recombinante que se conserva a una temperatura refrigerada de entre 2 y 8 grados centígrados, su logística y distribución a nivel mundial es más sencilla”.
Además añaden que se trata de una vacuna “lista para utilizar”, ya que no es necesario reconstituirla antes, lo que facilita la tarea del personal sanitario”.
Para la aprobación de una vacuna, conocida como precalificación, la OMS aplica los estándares internacionales para evaluar y determinar de forma exhaustiva si es segura y efectiva.
También lleva a cabo reevaluaciones, inspecciones, pruebas específicas e investigaciones periódicas a estas vacunas registradas dentro del Programa de Precalificación de Medicamentos (PQP).
Además de la aprobación de la OMS, la vacuna contra la COVID-19 de HIPRA cuenta con la de otras autoridades como la Agencia Europea del Medicamento (EMA), la Comisión Europea (CE) y la Agencia Reguladora de Medicinas y Productos Sanitarios del Reino Unido (MHRA).
Hipra es una empresa farmacéutica biotecnológica enfocada a la prevención para salud animal y humana, con una amplia gama de vacunas nnovadoras y un avanzado servicio de diagnóstico.
La compañía tiene una sólida presencia internacional con cuarenta filiales propias, tres centros de investigación y desarrollo y seis plantas de producción en Europa (España) y América (Brasil).